Журнальные публикации
полные тексты избранных публикаций
МЕТОДОЛОГИЧЕСКИЕ АСПЕКТЫ ИССЛЕДОВАНИЙ СВОБОДНОРАДИКАЛЬНОГО ОКИСЛЕНИЯ И АНТИОКСИДАНТНОЙ СИСТЕМЫ ОРГАНИЗМА
ЗАЙЦЕВ В.Г., ЗАКРЕВСКИЙ В.И.
Волгоградская медицинская академия, кафедра биохимии
Опубликовано в 1998 г. в журнале «Вестник Волгоградской медицинской академии».
В данной статье авторы рассматривают существующие сложности и противоречия в современных подходах к оценке свободнорадикальных процессов в живых организмах. На основании анализа взаимодействия в живой клетке реакций свободнорадикального окисления и компонентов системы антиоксидантной защиты предпринята попытка предложить метологию оценки этих взаимосвязей.
Ключевые слова: антиоксидантная защита, свободнорадикальное окисление, перекисное окисление липидов
Ключевые слова: антиоксидантная защита, свободнорадикальное окисление, перекисное окисление липидов
В настоящее время не вызывает сомнений, что процессы свободнорадикального окисления (СРО) играют чрезвычайно важную роль в жизнедеятельности клеток. Это связано с двумя основными моментами: с одной стороны, реакции СРО являются необходимым этапом различных метаболических процессов, а с другой стороны, повышенная интенсивность СРО во многих случаях является либо следствием, либо причиной тех или иных патологических изменений в клетках и тканях. В качестве примеров патологических состояний, развитие которых тесно связано со СРО, можно привести ревматические заболевания [3], атеросклероз [1], осложнения сахарного диабета (кардиомиопатия [11], нефропатия [6], ретинопатия [16]), амиотрофический боковой склероз [2], катаракту [14] . На сегодняшний день накоплен обширный фактический материал о взаимосвязи функциональной активности антиоксидантной системы (АОС) с интенсивностью СРО в физиологических условиях и при патологии [18]. Это существенно приблизило нас к пониманию, каким образом протекают и регулируются процессы СРО в живых организмах.
Тем не менее, существует несколько серьезных методологических проблем, заметно сдерживающих прогресс исследований в этой области. Во-первых, нет четкого определения, какие процессы могут быть отнесены к СРО. Некоторые авторы ограничивают СРО лишь реакциями перекисного окисления липидов (ПОЛ), хотя ПОЛ является только одной из составляющих частей СРО. Во-вторых, до сих пор во многих работах клинического плана для оценки интенсивности ПОЛ или СРО используются только один или два показателя без учета того, какие именно реакции СРО доминируют в конкретном случае, какие радикалы преимущественно вовлечены в рассматриваемые процессы. В ряде случаев это может приводить к существенным ошибкам в выводах. Наконец, само понятие АОС на сегодня более чем расплывчато. Во всяком случае, нам не удалось обнаружить в изученных литературных источниках обоснованного и достаточно полного списка компонентов АОС и их функциональной роли. Само же функционирование компонентов АОС часто рассматривается изолированно от остальных метаболических систем клеток. Мы полагаем, что решение указанных проблем позволило бы проводить более целенаправленные исследования роли реакций СРО и АОС в норме и при патологии.
В настоящей работе мы попытались предложить некоторые подходы к решению методологических аспектов изучения процессов СРО и функционирования АОС в клетке.
В живых организмах в процессе биологического окисления постоянно образуются различные активные формы кислорода (АФК) [4]. Основным источником их в живой клетке являются оксидоредуктазы, в процессе функционирования которых всегда образуется некоторое количество супероксид-анион-радикала •О2– и пероксида водорода Н2О2, а также процессы автоокисления некоторых низкомолекулярных веществ (например, катехоламинов). В концентрациях, обнаружимых в живых клетках, токсическим действием обладает •О2– [9] , но не Н2О2. Возможно, главную роль играет продукт взаимодействия Н2О2 и •О2– – гидроксил-радикал •OH [7], который в настоящее время считается наиболее токсичной АФК. Радикальные АФК способны эффективно окислять (и тем самым инактивировать) различные белки, разрушать некоторые полисахариды и стимулировать мутагенез (за счет накопления окислительных повреждений в ДНК). Важным свойством АФК является их способность инициировать перекисное окисление жирных кислот и жирнокислотных остатков в составе липидов (процессы ПОЛ). При этом перекисное окисление различных жирных кислот может протекать с разным соотношением между отдельными путями развития ПОЛ и с образованием разных продуктов. Например, большая часть арахидоновой кислоты окисляется до малонового диальдегида, а продуктом перекисного окисления линоленовой кислоты является главным образом 4-гидрокси-2-ноненаль, но не малоновый диальдегид. Карбонильные продукты ПОЛ легко образуют аддукты с нуклеиновыми кислотами и многими белками (в том числе с ферментами АОС, вызывая их инактивацию). Наиболее существенные этапы процесса СРО в живой клетке указаны на приведенной ниже схеме. Легко видеть, что в развитии и проявлении токсичности реакций СРО принимают участие все АФК и почти все продукты СРО.
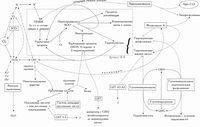 | Рисунок. Схема взаимодействия процессов свободнорадикального окисления и ферментов антиоксидантной защиты. Загрузить в полный размер (44 кб): в этом окне | в новом окне |
Компоненты АОС характеризуются специфическим действием на различные звенья СРО. Так, существуют ферменты, направленно утилизирующие АФК (супероксиддисмутаза – СОД, каталаза, пероксидазы), продукты ПОЛ, участвующие в развитии СРО (глутатионпероксидазы – ГП), и токсические продукты СРО (глутатион-S-трансферазы – ГТ). До сих пор, правда, не обнаружено компонента АОС, который бы специфически утилизировал *ОН. При этом защита клеточных структур от повреждающего действия АФК, продуцирующихся внутри клетки (эндогенные АФК) и воздействующих извне (экзогенные АФК) организуется различным образом. В первую очередь это связано с неспособностью АФК проникать сквозь мембраны. В результате экзогенные АФК всегда воздействуют на клетку только опосредованно через стимуляцию ПОЛ в плазматической мембране. Поэтому защита от повреждения экзогенными АФК направлена в первую очередь на утилизацию жирнокислотных и липидных гидропероксидов, как продуктов ПОЛ, стимулирующих СРО по принципу цепной реакции. Основная роль в этой защите принадлежит ГП, особенно, специфической ГП гидропероксидов фосфолипидов. Сверхэкспрессия в клетках различных форм ГП (но не СОД) приводит к значительному повышению устойчивости клеток к экзогенным окислителям [5, 19] . Часть радикальных продуктов в мембране перехватывается SH-группами мембранных белков, часть (главным образом, вблизи внешней поверхности мембраны) токоферолами. Последние могут затем регенерироваться на внутренней стороне мембраны за счет передачи окислительных эквивалентов на цитозольный аскорбат [12]. Фосфолипиды с перекисно-окисленными жирнокислотными остатками являются более предпочтительным субстратом для фосфолипазы А2, чем нормальные неокисленные фосфолипиды [13]. Образующиеся в результате лизофосфолипиды вновь ацилируются при участии ацилтрансферазы. Отщепившиеся гидропероксиды жирных кислот утилизируются низкоспецифическими формами ГП. Такой механизм репарации окисленных липидов позволяет снизить вредное влияние ПОЛ на физическую структуру плазматической мембраны. Образовавшиеся карбонильные продукты утилизируются в цитозоле, а конъюгированные диены, триены и продукты рекомбинации липидных радикалов, по-видимому, не утилизируются, а накапливаются в клетках вместе с окисленными белками в виде «липофуциновых гранул» [17]. Аналогичная система защиты мембраны от ПОЛ существует в митохондриях.
Напротив, защита от эндогенных АФК основана главным образом на эффективной элиминации первичных АФК. Для этого служат СОД, каталаза и пероксидазы (в том числе низкоспецифические ГП). Поскольку СОД утилизирует •OH с образованием Н2О2, важным для жизнеспособности клетки оказывается баланс между активностями СОД и ферментов, разрушающих Н2О2: резкое повышение в клетке активности СОД (путем специфической активации или сверхэкспрессии) без соответствующей активации каталазы или пероксидаз само по себе является цитотоксичным [15]. Поскольку в цитозоле основной мишенью для АФК являются белки, важную роль в защите от эндогенных АФК играют восстановленный глутатион (GSH) и цистеин. SH-группы этих веществ окисляются гораздо легче, чем SH-группы в белковых молекулах, защищая тем самым белки от окислительной модификации. Приведенные факты позволяют вполне обоснованно говорить, что клеточная АОС достаточно четко подразделяется на подсистему защиты от эндогенных АФК и подсистему защиты от повреждающего действия экзогенных АФК.
По-видимому, в составе АОС можно выделить также подсистему детоксикации продуктов СРО и поврежденных компонентов клетки. В первую очередь к этой подсистеме следует отнести ГТ. Семейство ГТ является, собственно, важнейшим компонентом системы детоксикации токсических метаболитов и ксенобиотиков. В то же время, существуют изоферменты, которые обладают высокой активностью в отношении продуктов СРО [8]. Так, ГТ 5-5 крысы высокоактивна в отношении продуктов окислительной модификации нуклеотидов и нуклеиновых кислот и является единственной изоформой обнаруживаемой почти исключительно в ядре клетки. ГТ А3-А3 мыши способен к эффективной детоксикации гидропероксидов жирных кислот, а некоторые изоформы ГТ – к продукции конъюгатов GSH с 4-гидроксиалкеналями. Кроме того, экспрессия различных форм ГТ может повышаться параллельно с интенсификацией СРО в клетке.
Функционирование различных компонентов АОС требует тесного взаимодействия с другими системами клеточного метаболизма. В первую очередь это связано с существенной зависимостью АОС от наличия достаточного количества GSH. Для регенерации окисленного глутатиона в GSH в клетках присутствует глутатионредуктаза (ГР). Ферментативное восстановление глутатиона зависит от NADPH, поэтому функционирование GSH-зависимых компонентов АОС тесно связано с активностью NADPH-продуцирующих ферментов. Неслучайно, что интенсификация СРО приводит к активации в клетке не только ферментов АОС и ГР, но и ферментов пентозофосфатного пути [10]. Для работы системы репарации липидов требуется постоянное наличие в клетке резервного пула жирных кислот, связанных с коферментом А. Важную роль играет также микросомальная система регенерации токоферолов.
Таким образом, в протекание реакций СРО в клетках вовлечено большое число различных веществ, еще большее число компонентов клетки участвует в регуляции уровня СРО. Поэтому изолированное изучение отдельных компонентов АОС клетки и/или содержания одного-двух продуктов ПОЛ для целей исследования механизма развития и регуляции СРО представляется нам недостаточно информативным и, соответственно, мало целесообразным. В то же время, в каждом конкретном случае выбор исследуемых звеньев СРО и компонентов АОС должен быть целенаправленным, необходимым, достаточным и адекватным поставленным задачам. Это особенно важно в клинических и патофизиологических исследованиях. Например, при исследованиях защиты от повреждающего действия экзогенных АФК мы рекомендуем проводить в качестве основных тестов одновременное определение содержание гидропероксидов, карбонильных продуктов ПОЛ и GSH, а также активности фосфолипазы А2 и ГП. При изучении процессов, связанных с эндогенной продукцией АФК, наиболее информативным будет определение активности СОД, Н2О2-утилизирующих ферментов, ГТ и содержания GSH. Оценка степени повреждения компонентов клетки возможна при определении содержания аддуктов карбонильных продуктов ПОЛ с белками и 8-гидроксидезоксигуанозина (показатель окислительного повреждения ДНК).
В то же время, при исследовании отдельных звеньев процесса СРО и компонентов АОС in vitro нам кажется целесообразным использовать модельные системы из 3 составных частей (модулей): химической системы генерации АФК (или АФК и продуктов СРО); компонентов селективной элиминации определенных АФК или продуктов СРО и системы индикации. Использование модельной системы позволяет более тщательно изучить отдельные стадии СРО и взаимодействие тех или иных компонентов клетки с различными АФК и продуктами СРО. Такая модульная структура позволяет за счет использования различных сочетаний определенных отдельных составляющих частей создать систему, приспособленную для изучения практически любой реакции СРО, действия определенного вида АФК или функционирования конкретного компонента АОС.
В качестве примера возможности использования модельной системы можно привести результаты наших исследований воздействия АФК на замещенные фенолы, включая катехоламины, с последующим развитием СРО. Задачей исследования было изучение эффективности инициации СРО этих соединений отдельными видами АФК. Модельная система состояла из первого и третьего модулей. В качестве системы генерации использованы водные растворы Н2О2 (как отдельный вид АФК), (NH4)2S2O8 (для генерации •О2–) или смеси NADH с феназинметосульфатом (для генерации спектра АФК, близкого к образующемуся в живых клетках). При использовании для индикации электрохимической и спектрофотометрической детекции продуктов окисления адреналина и норадреналина было обнаружено, что различные виды АФК не только с различной эффективностью инициируют СРО катехоламинов, но и стимулируют образование различного набора продуктов СРО. Это говорит о том, что различные АФК могут инициировать развитие процесса СРО преимущественно по различным путям, что и приводит к образованию различных конечных продуктов. Кроме того, было показано, что использование электрохимического и спектрофотометрического определения взаимно дополняет друг друга, поскольку электрохимически может быть дополнительно выявлено образование неокрашенных продуктов СРО.
Полученные нами результаты свидетельствуют о перспективности применения модельных систем предложенного типа для изучения конкретных реакций СРО и компонентов АОС in vitro.
ЛИТЕРАТУРА
- Benzie I.F. Int. J. Food Sci. Nutr. 1996. V.47. N 3. P.233 – 261
- Bergeron C. J. Neurol. Sci. 1995. V.129, suppl. P.81 – 84
- Berliner J.A., Heinecke J.W. Free Radic. Biol. Med. 1996. V.20. N 5. P.707 – 727
- Davies K.J. Biochem. Soc. Symp. 1995. V.61. P.1 – 31
- Doroshow J.H. Toxicol. Lett. 1995. V.82–83. P.395 – 398
- Ha H., Kim K.H. Kidney Int. 1995. V.51, suppl. P.S18 – S21
- Halliwell B., Gutteridge J.M.C. Arch. Biochem. Biophys. 1986. V.246. N 2. P.501 – 506
- Hayes J.D., Pulford D.J. Crit. Rev. Biochem. Mol. Biol. 1995. V.30. N 6. P.445 – 600
- Implay J.A., Fridovich I. J. Biol. Chem. 1991. V.266. N 11. P.6957 – 6965
- Kashiwagi A., Asahina T., Nishio Y., Ikebuchi M., Tanaka Y., Kikkawa R., Shigeta Y. // Diabetes. 1996. V.45. Suppl. 3. P.S84 – S86
- Kaul N., Sivelski-Iliskovic N., Thomas T.P., Hill M., Khaper N., Singal P.K. Nutrition. 1995. V.11. N 5, suppl. P.551 – 554
- May J.M., Qu C., Morrow J.D. J. Biol. Chem. 1996. V.271. N 18. P.10577 – 10582
- McLean L.R., Hagaman K.A., Davidson W.S. Lipids. 1993. V.28. N 6. P.505 – 509
- Obara Y. Nippon Ganka Gakkai Zashi. 1995. V.99. N 12. P.1303 – 1341
- Peskin A.V. Biosci. Rep. 1997. V.17. N 1. P.85 – 89
- Rema M., Mohan V., Bhaskar A., Shanmugasundaram K.R. Indian J. Ophthalmol. 1995. V.43. N 1. P.17 – 21
- Tappel A.L., Fletcher B., Deamer D. J. Gerontol. 1973. V.28. N 3. P.415 – 420
- Winterbourn C.C. Clin. Exp. Pharmacol. Physiol. 1995. V.22. N 11. P.877 – 880
- Yagi K., Komura S., Kojima H., Sun Q., Nagata N., Ohishi N., Nishikimi M. Biochem. Biophys. Res. Commun. 1996. V.219. N 2. P.486 – 491
оформление библиографической ссылки
Зайцев В.Г., Закревский В.И. Методологические аспекты исследований свободнорадикального окисления и антиоксидантной системы организма // Вестник Волгоградской медицинской академии (ВМА; Тр., т.54, вып.4)– Волгоград, 1998.– С.49-53.
