|
Министерство здравоохранения и социального развития Российской Федерации
Государственное образовательное учреждение высшего профессионального образования Волгоградский государственный медицинский университет
RUS
» ENG
|
 |
|
Наука в ВолГМУ >> Научные конференции >> Современная фармакотерапия вирусных инфекций >> Озерова с соавт.
|
обновлено 23.12.2024 |
|
|
Современная фармакотерапия вирусных инфекций
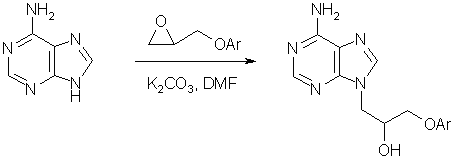
3: Химический синтез противовирусных лекарственных веществ СИНТЕЗ И ПРОТИВОВИРУСНАЯ АКТИВНОСТЬ НОВЫХ ПРОИЗВОДНЫХ 9-(2,3-ДИГИДРОКСИПРОПИЛ)АДЕНИНА Озерова Т.П., Брель А.К., Новиков М.С., Солодунова Г.Н., Павлова И.Ю. Кафедра химии ВолГМУ, кафедра фармацевтической и токсикологической химии ВолГМУ S-Аденозил-L-гомоцистеингидролаза является ключевым ферментом в реакциях метилирования нуклеиновых кислот, катализирующим гидролиз S-аденозил-L-гомоцистеина до аденозина и гомоцистеина. Многие вирусы чувствительны к ингибиторам S-аденозил-L-гомоцистеингидролазы, в связи с чем на их основе возможно создание противовирусных агентов с широким спектром действия. Наиболее перспективными ингибиторами этого фермента, несомненно, являются производные аденина, имеющие как нуклеозидную, так и ненуклеозидную природу. Основным методом синтеза новых 3-О-ариловых эфиров (R,S)-9-(2,3-дигидроксипропил)аденина послужило алкилирование аденина-основания арилглицидиловыми эфирами в среде безводного диметилформамида при температуре 105-110°С в присутствии карбоната калия. Исходные арилглицидиловые эфиры были получены путем взаимодействия эпихлоргидрина с соответствующими фенолами в щелочной среде [1].
где Ar = фенил, п-хлорфенил, п-метилфенил, 1-нафтил, 2-нафтил. Согласно данным спектроскопии ПМР и тонкослойной хроматографии, реакция алкилирования калиевой соли аденина использованными эпоксидами протекает в указанных условиях с высокой региоселективностью и не приводит к побочным 7-замещенным производным аденина. Синтезированные 3-О-ариловые эфиры (R,S)-9-(2,3-дигидроксипропил)аденина хорошо растворимы в кислотах, этаноле, диметилсульфоксиде и представляют интерес в качестве потенциальных противовирусных средств. Противовирусные и цитотоксические свойства in vitro новых ариловых эфиров (R,S)-9-(2,3-дигидроксипропил)аденина были изучены в Рега институте медицинских исследований (Католический университет, г. Лювен, Бельгия) в отношении широкого ряда ДНК- и РНК-содержащих вирусов. Было обнаружено, что родоначальник данного ряда соединений - (R,S)-9-(3-фенокси-2-гидроксипропил)аденин проявляет активность в отношении Коксаки вируса В4 (ЕС50 = 240 мкг/мл) при величине цитотоксичности свыше 400 мкг/мл. Фенилглицидиловый эфир. К раствору 40,0 г (0,425 моль) фенола и 26,5 г (0,425 моль) 90 %-ного КОН в 100 мл воды добавляют при начальной температуре 20-25°С 40,0 мл (0,511 моль) свежеперегнанного эпихлоргидрина и интенсивно перемешивают в течение 30 мин, постепенно повышая температуру раствора до 90-95°С. После достижения указанной температуры реакционную массу перемешивают еще 15 мин, охлаждают до комнатной температуры, добавляют 100 мл бензола, органический слой отделяют, промывают 100 мл воды, сушат сульфатом натрия, фильтруют и упаривают на кипящей водяной бане в вакууме водоструйного насоса. Остаток перегоняют в вакууме, собирая фракцию с Т.кип. 131-134 оС (10 мм рт.ст.), n20D 1,5312, выход 51,7 г (81,0 %). ПМР-спектр, δ, м.д. (ацетон-D6): 2,41 дд (5 Гц, 2 Гц, 1 Н, СН2-транс); 2,56 т (5 Гц, 1 Н, СН2-цис); 2,92-3,14 м (1 Н, СН); 3,52-4,00 м (2 Н, ОСН2); 6,56-6,80 м (3 Н, фенил); 6,89-7,14 м (2 Н, фенил). (R,S)-9-(3-Фенокси-2-гидроксипропил)аденин. Смесь 1,5 г (11,1 ммоль) аденина и 1,6 г (11,6 ммоль) свежепрокаленного карбоната калия перемешивают в течение 1 ч при температуре 105-110°С в 40 мл безводного диметилформамида, добавляют раствор 1,7 г (11,3 ммоль) фенилглицидилового эфира в 10 мл диметилформамида и перемешивают при той же температуре в течение 2 ч. Охлаждают, фильтруют, фильтрат упаривают в вакууме, остаток дважды перекристаллизовывают из 50 мл 2-пропанола и получают 2,2 г (69,4 %) целевого продукта в виде белого кристаллического вещества, Т.пл. 169-172°С. ПМР-спектр, δ, м.д. (диметилсульфоксид-D6): 3,77-4,01 м (2 Н, N-CH2); 4,09-4,48 м (3 Н, ОСН2СН); 5,43 уш.с (1 Н, ОН); 6,67-7,28 м (5 Н, фенил), 7,03 уш.с (2 Н, NH2); 7,95 с (1 Н, Н2); 8,05 c (1 Н, Н8). |
||